Welche Rolle O-GlcNAc spielt
Proteinmodifikationen
Ein Großteil der Proteine in unseren Zellen trägt kleine Anhängsel aus Zuckermolekülen, die wichtig für ihre Funktion sind. Das O-gebundene N-Acetylglucosamin ist sogar so wichtig, dass unsere Zellen ohne es gar nicht überleben könnten. Forscher am Max-Planck-Institut für Biochemie in Martinsried haben nun einen bisher ungekannten Mechanismus entdeckt, der erklärt wie diese Zuckerreste auf die Proteine wirken und wie sie dadurch die Entwicklung unseres Körpers beeinflussen können.
Warum das O-gebundene N-Acetylglucosamin oder O-GlcNAc so wichtig ist, ist bisher noch nicht ganz klar. Die Wissenschaftler Maria Cristina Gambetta und Jürg Müller am Max-Planck-Institut für Biochemie haben sich dieser Frage aber nun genähert, indem sie versuchten, einzelne wichtige Moleküle zu identifizieren, die ohne GlcNAc nicht mehr funktionieren. Die Verwendung des Modellorganismus Drosophila, der Fruchtfliege, hat ihnen genau dies ermöglicht.
Die Forscher konnten zeigen, dass Fliegen, deren Zellen kein GlcNAc an die Proteine anhängen können, schwere Störungen in ihrer Entwicklung aufwiesen: konkret „vergaßen“ die Zellen schlichtweg, welches Körperteil sie zu bilden hatten. „Dieses Phänomen war uns schon von Experimenten mit anderen Proteinen bekannt“, erklärt Maria Cristina Gambetta, Erstautorin der Studie. „Zellen denen Proteine der sogenannten Polycomb-Gruppe fehlen, zeigen genau diese Art von Störungen“. Polycomb Proteine sind so etwas wie das molekulare Gedächtnis der Zellen. Sie schalten gezielt einzelne Gene aus und bestimmen so das Schicksal und die künftigen Aufgaben der Zelle. Doch wie passten diese beiden Ergebnisse zusammen?
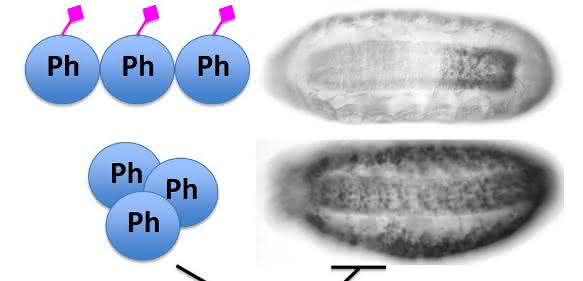
In weiteren Analysen fanden die Wissenschaftler heraus, dass ein bestimmtes Polycomb-Protein mit dem Namen Polyhomeotic, kurz Ph, unbedingt auf den GlcNAc Zuckeranhang angewiesen ist. Dies hängt laut den Forschern vor allem damit zusammen, dass die einzelnen Ph-Moleküle ohne die GlcNAc-Anhängsel ungeordnet aneinander geraten und verklumpen. In dieser Form kann Ph keine Genaktivitäten mehr regeln und verliert daher seinen Einfluss auf das Schicksal der Zellen. „Der Mechanismus, dass GlcNAc-Moleküle ein Verklumpen von Proteinen verhindern, war bisher noch völlig unbekannt“, ordnet Jürg Müller die Ergebnisse ein. „Zudem konnten wir zeigen, dass dies der wichtigste auf GlcNAc beruhende Prozess in der Fruchtfliege ist.“
In der aktuellen Studie konnten die Wissenschaftler zeigen, dass das menschliche Ph-Protein, welches große Ähnlichkeiten mit dem Fruchtfliegen-Ph hat, beim Fehlen der Zuckeranhängsel ebenfalls verklumpt. „Es wird spannend sein, nun zu sehen, welche Auswirkungen das Fehlen von GlcNAc auf die verschiedenen biologischen Prozesse hat, die durch Ph geregelt werden“, so Maria Cristina Gambetta. ´
Originalpublikation
M.C. Gambetta and J. Mu?ller: O-GlcNAcylation Prevents Aggregation of the Polycomb Group Repressor Polyhomeotic. Developmental Cell, November 26, 2014.
DOI:10.1016/j.devcel.2014.10.020.