Wie Zellen Gewebe bilden
Zellskelett an der Bildung von Epithelien beteiligt
Wie haften die Zellen eines Gewebes aneinander? Der Antwort auf diese Frage ist ein Pharmakologenteam von der Philipps-Universität Marburg jetzt nähergekommen: Die Wissenschaftlerinnen und Wissenschaftler um Prof. Dr. Robert Grosse fanden heraus, dass das Molekül Formin-like 2 (FMNL2) gebraucht wird, um Zellen miteinander zu verbinden.
„Unversehrte Deckgewebe – sogenannte Epithelien – sind lebenswichtig“, betont Studienleiter Grosse; sie kleiden zum Beispiel die Blutgefäße aus. Die korrekte Bildung dieser Gewebe ist auch medizinisch von Belang, hebt der Pharmakologe hervor: „So entstehen Krebserkrankungen oftmals aus geschädigten Epithelien.“
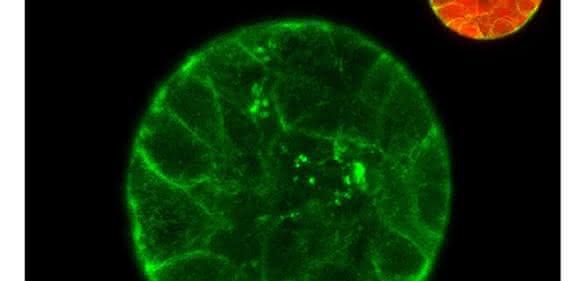
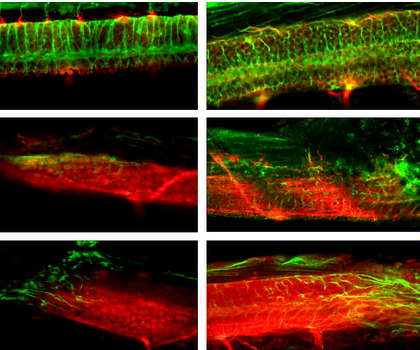
Damit flächige Deckgewebe entstehen, bilden sich zwischen den einzelnen Zellen Haftkomplexe (adherens junctions, AJ), die mehrere Proteine umfassen. „Im intakten Gewebe sind diese Zell-Zell-Kontakte mit dem Zellskelett verbunden, das aus Aktin besteht“, erklärt Grosse; „aber wo dieses Aktin herkommt und wie es reguliert ist, war bisher nicht vollständig geklärt.“
Um die offenen Fragen zu beantworten, experimentierten die Autoren mit Zellen unter natürlichen Wachstumsbedingungen und beobachteten die beteiligten Moleküle in Echtzeit. Das Team verwendete für seine Studien ein Substrat, das die dreidimensionale Ausbreitung des Gewebes erlaubt.
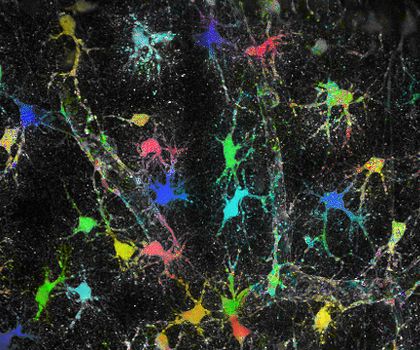
Grosse und seine Mitarbeiter identifizierten einen Faktor, der an den Kontaktstellen zwischen Epithelzellen des menschlichen Körpers dafür sorgt, dass Gerüste aus Aktin entstehen: Formin-like 2 (FMNL2). Wie die Autoren ermittelten, reichert sich FMNL2 an den Kontaktstellen an, durch die sich Zellen zu einem Epithel verbinden.
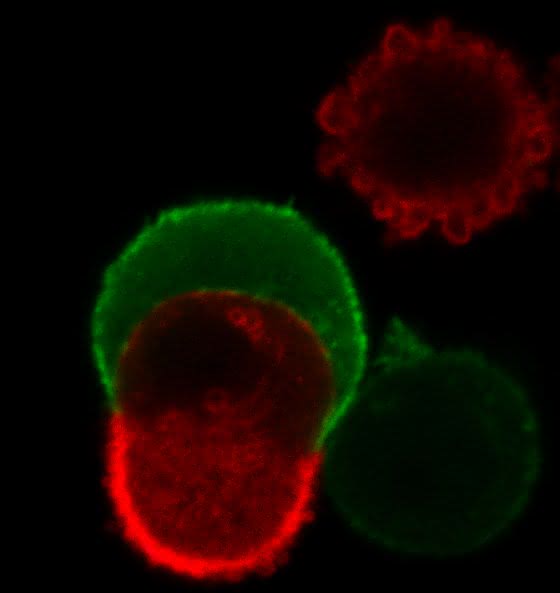
Auslöser für Zell-in-Zell-Invasionen...
Gerüstet für die Invasion
Rückendeckung für Eindringlinge: Das Gerüstprotein Aktin reichert sich an der Rückseite einer Zelle an, wenn diese in eine andere Zelle eindringt. Das haben Pharmakologen von der Philipps-Universität herausgefunden, als sie nach Molekülen suchten, die an Zell-in-Zell-Invasionen (Entosis) beteiligt sind.
Welche Funktion hat FMNL2 für die Bildung des Aktingerüstes? Dies untersuchte das Team, indem es das FMNL2-Gen ausschaltete – das Ergebnis: Die Aktin-Ketten, aus denen das Gerüst an den Anheftungsstellen entsteht, sind unterbrochen. Schließt das gebildete Epithel einen Hohlraum ein, so ist dieser missgebildet. Ein künstliches FMNL2-Protein kann die Funktion des fehlenden natürlichen Moleküls ersetzen.
Die Wissenschaftlerinnen und Wissenschaftler fanden auch heraus, dass FMNL2 mit den Bestandteilen des Haftkomplexes zusammenwirkt, zum Beispiel mit den Proteinen E-Cadherin und Rac1. Außerdem wollten die Autoren wissen, wer die Aktivität von FMNL2 steuert. Die Arbeitsgruppe griff hierfür auf eine Methode zurück, die Grosses Labor kürzlich benutzt hat, um Moleküle mittels Licht gezielt zu aktivieren. Dabei zeigte sich – live und in Farbe –, dass FMNL2 als auch Aktin-Filamente sich innerhalb kürzester Zeit an den Kontaktzonen der Zellen anreichert, nachdem Rac1 angeschaltet wird.
„Das Protein Formin-like 2 ist in vielen Epithelien des menschlichen Körpers vorhanden“, erklären die Autoren zur Bedeutung ihrer Resultate. Die Fehlbildung solcher Gewebe kann zu Krebs führen, etwa zu Brustkrebs. „Wie FMNL2 mit dem Haftkomplex im Detail zusammenwirkt und welche weiteren Moleküle die Haftung zwischen Zellen beeinflussen, muss in künftigen Untersuchungen geklärt werden“, schreibt das Wissenschaftlerteam.
Prof. Dr. Robert Grosse ist Direktor des Pharmakologischen Instituts am Fachbereich Medizin der Philipps-Universität und leitet einen Arbeitsbereich am Biochemisch-Pharmakologischen Centrum der Philipps-Universität. Die zugrunde liegende Forschungsarbeit wurde durch die Deutsche Forschungsgemeinschaft im Rahmen des Schwerpunktprogramms SPP 1782 finanziell gefördert.
Originalveröffentlichung:
Katharina Grikscheit & al.: Junctional actin assembly is mediated by Formin-like 2 downstream of Rac1, J. Cell Biol. 2015.
Weitere Informationen:
Prof. Dr. Robert Grosse
Pharmakologisches Institut und Biochemisch-Pharmakologisches Centrum Marburg
E-Mail: [email protected]
Homepage: www.bpc-marburg.de/cytoskeletal-signaling-grosse-lab/