Amyotrophe Lateralsklerose und frontemporale Demenz
Toxische Arginin-haltige Proteine schädigen Nervenzellen
Jüngste Erkenntnisse der biomedizinischen Grundlagenforschung könnten den Weg zu neuen Therapien gegen ALS und einer speziellen Form von Demenz ebnen. Denn in welcher Weise eine genetische Mutation zu neuronalen Schäden bei diesen zwei schweren Krankheiten führt, haben jetzt Wissenschaftler am Max-Planck-Institut für Biologie des Alterns in Köln und des University College London herausgefunden. In seltenen Fällen leiden Patienten gleichzeitig unter amyotropher Lateralsklerose (ALS) und frontemporale Demenz. Bislang war jedoch nicht bekannt, was beide Krankheiten auslöst.
ALS ist eine folgenschwere Motoneuronerkrankung, die rasch zu einer Schwächung der Muskulatur und schließlich zum Tod führt. Frontotemporale Demenz ist die zweithäufigste Ursache von Demenz bei Menschen unter 65 Jahren. Zu den Symptomen zählen Veränderungen in Persönlichkeit und Verhalten sowie Sprach- und Denkschwierigkeiten.
Die DNA betroffener Patienten enthält eine Mutation im C9orf72 Gen: Es gibt Tausende von Wiederholungen eines bestimmten, kurzen Abschnitts des genetischen Materials, während die DNA nicht betroffener Personen nur bis zu dreißig Kopien dieses Segments aufweist. Diese spezifische genetische Veränderung liegt der Erkrankung bei etwa 8 % der Patienten mit dieser Art von Motoneuronkrankheit oder Demenz zugrunde. 8 % ist ein relativ hoher Anteil. Bei der Alzheimer-Erkrankung beispielsweise machen die genetischen Ursachen der Erkrankung weniger als 1 % aus.
Forscher am Max-Planck-Institut für Biologie des Alterns, des Instituts für Neurologie und des "Institute for Healthy Ageing" am University College London haben nun gemeinsam herausgefunden, dass die Neurodegeneration bei diesen Krankheiten durch toxische Proteine ausgelöst wird, die aufgrund der Wiederholungen im mutierten Gen erzeugt werden.
Fruchtfliegen und Menschen: ähnliche Art der Neurodegeneration
Bisher ging man davon aus, dass die Schäden eine Folge der Unterbrechung des Gens durch die abnormen Wiederholungen sein könnten. Oder dass durch die Wiederholungen toxische Ribonukleinsäure (RNA) erzeugt wird. Nun stellte sich heraus, dass die Wiederholungen in dem mutierten Gen zur Produktion einer Vielzahl von Proteinen führen, und dass zwei von diesen extrem schädlich für Nervenzellen sind. Beide sind sehr reich an der Aminosäure Arginin.
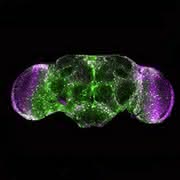
Um genau herauszufinden, welche Rolle die Proteine spielen, stellten die Forscher künstliche Wiederholungen in der DNA her: Wiederholungen, die zugleich potenziell toxische RNA und Proteine erzeugten - und Wiederholungen, die nur zur Produktion potenziell toxischer RNA oder nur zur Produktion der Proteine führten. Diese künstlich erzeugten Wiederholungen brachten sie in die Nervenzellen von Fruchtfliegen ein, in denen Abbau von Nervenzellen in ähnlicher Weise abläuft wie im Menschen.
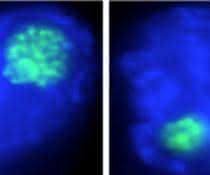
Das Ergebnis: Wiederholungen in der DNA, die zugleich potenziell schädliche RNA und Proteine bedingt, führten zu einer starken Schädigung der Nervenzellen und reduzierten die Lebensdauer der Fliegen. Interessanterweise verursachten die Wiederholungen, die ausschließlich zur Produktion der Proteine führten, eine genauso markante Neurodegeneration. Keine Schäden dagegen zogen die Wiederholungen mit sich, die ausschließlich RNA erzeugten. Somit war die toxische Wirkung der Proteine nachgewiesen. Dabei richteten die stark Arginin-haltigen Proteine den größten Schaden an.
Mit ihren Ergebnissen haben die Kölner und Londoner Forscher ein neues Licht auf die toxische Rolle Arginin-haltiger Proteine bei Motoneuronerkrankungen und Demenz geworfen. Ihre Erkenntnisse könnten künftig bei der Entwicklung von Medikamenten gegen diese schweren Leiden helfen.
Originalpublikation:
Sarah Mizielinska, Sebastian Grönke, Teresa Niccoli, Charlotte E. Ridler, Emma L. Clayton, Anny Devoy, Thomas Moens, Frances E. Norona, Ione O.C. Woollacott, Julian Pietrzyk, Karen Cleverley, Andrew J. Nicoll, Stuart Pickering-Brown, Jacqueline Dols, Melissa Cabecinha, Oliver Hendrich, Pietro Fratta, Elizabeth M.C. Fisher, Linda Partridge, Adrian M. Isaacs: C9orf72 repeat expansions cause neurodegeneration in Drosophila through arginine-rich proteins. Science Express, 7. August 2014.
Ansprechpartner:
Dr. Sebastian Grönke
Max-Planck-Institut für Biologie des Alterns, Köln
E-Mail: [email protected]