Multiresistente Keime
Resistenzen bei der Konkurrenz besorgt
Forscher an der Universität Basel konnten zeigen, dass einige Bakterien ihren Konkurrenten einen Giftcocktail injizieren, der diese zerplatzen lässt. Die dabei freigesetzte Erbinformation, die auch Resistenzgene enthalten kann, nimmt das Angreifer-Bakterium auf und wird so selbst resistent.
Die häufige und oftmals unachtsame Verwendung von Antibiotika führt zu einer immer schnelleren Verbreitung von Resistenzen. Zu den Hot-Spots zählen dabei insbesondere Spitäler. Hier bringen nicht nur Patienten unterschiedlichste, zum Teil bereits resistente Keime ins Haus. Durch den Einsatz von Antibiotika zur Bekämpfung von Infektionen sind Spitäler ein Ort, wo Antibiotika-Resistenzen häufiger entstehen und zusätzlich unter den bakteriellen Krankheitserregern weitergegeben werden.
Einer dieser typischen Krankenhauskeime ist das Bakterium Acinetobacter baumannii. Umgangssprachlich wird es auch als Irak-Keim bezeichnet, da im Irakkrieg multiresistente Bakterien dieser Art schwere, nur schwer behandelbare Wundinfektionen bei amerikanischen Soldaten verursachten.
Multiresistente Bakterien durch Genaustausch
Die Entstehung von Multiresistenzen geht unter anderem auf eine besondere Fähigkeit einiger Bakterien zurück: Sie bekämpfen Konkurrenten, indem sie ihnen Giftproteine, sogenannte Effektoren, mithilfe eines Typ-VI-Sekretionssystems (T6SS) injizieren. Die Angreifer sind in der Lage, die freiwerdende Erbsubstanz aufzunehmen und selbst wiederzuverwenden.
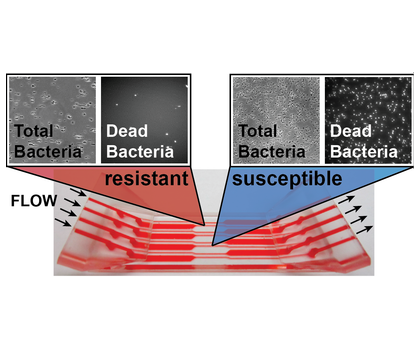
Im Modellorganismus Acinetobacter baylyi, einem nahen Verwandten des Irak-Keims, hat Prof. Marek Baslers Team vom Biozentrum der Universität Basel nun fünf solcher Effektoren identifiziert, die auf unterschiedlichste Art und Weise wirken. „Einige dieser toxischen Proteine töten den Gegner sehr effektiv, zerstören die Zelle dabei jedoch nicht“, erklärt Basler. „Andere wiederum beschädigen die Zellhülle so stark, dass das angegriffene Bakterium zerplatzt und Erbsubstanz austritt.“
Die Angreifer verleiben sich die freigesetzten DNA-Fragmente ein. Befinden sich darauf nun Gene, die für eine bestimmte Resistenz verantwortlich sind, so wird der neue Besitzer ebenfalls resistent gegen dieses Antibiotikum. Das Antibiotikum ist in Folge dessen nicht mehr wirksam und der Keim kann sich weitgehend ungestört vermehren.
In Spitälern sind Krankheitserreger mit diesen Fähigkeiten ein großes Problem. Denn durch den Kontakt mit anderen resistenten Keimen können diese immer neue Antibiotika-Resistenzen ansammeln – die Bakterien werden schließlich multiresistent. Im schlimmsten Fall wirkt kein Antibiotikum mehr, Infektionen mit multiresistenten Krankenhauskeimen werden zur tödlichen Gefahr für die Patienten.
Giftproteine und Gegengifte
„Das Typ-VI-Sekretionssystem sowie ein Set an verschiedenen Effektoren findet sich auch bei anderen Infektionserregern wie zum Beispiel dem Erreger der Lungenentzündung oder dem Choleraerreger“, sagt Basler. Interessanterweise wirken nicht alle Giftproteine gleich gut, da viele Bakterien Gegengifte – sogenannte Immunitätsproteine – entwickelt oder erworben haben.
„Wir haben für die fünf Effektoren auch die dazugehörigen Immunitätsproteine identifiziert. Für die Angreifer ist es sinnvoll, nicht nur ein einziges Giftprotein zu produzieren, sondern einen Cocktail verschiedenster Toxine mit unterschiedlicher Wirkungsweise“, so Basler. „So erhöht sich die Wahrscheinlichkeit, dass der Gegner erfolgreich ausgeschaltet werden kann und in einigen Fällen, durch die Auflösung der Zelle, auch dessen DNA verfügbar wird.“
Eroberung neuer ökologischer Nischen
Antibiotika und Resistenzen gibt es schon seit Jahrmillionen. Sie haben sich im Zusammenleben der Mikroorganismen entwickelt und ermöglichen Bakterien, sich gegen Feinde zu wehren oder Konkurrenten auszuschalten. Auf diese Weise können sie neue ökologische Nischen erobern und besetzen. Mit dem Einsatz von Antibiotika in der Medizin wurde die natürliche Fähigkeit zur Resistenzentwicklung jedoch zum Problem. Sie stellt die Forscher vor die Herausforderung, kontinuierlich neue Antibiotika zu entwickeln und die Ausbreitung der Resistenzen zu verlangsamen.
Originalbeitrag
Peter D. Ringel, Di Hu, Marek Basler. The role of Type VI Secretion System Effectors in Target Cell Lysis and Subsequent Horizontal Gene Transfer. Cell Reports (2017), doi: 10.1016/j.celrep.2017.12.020