Neuro-Implantate und Biochips
Geometrie von 3D-Nanoelektroden beeinflusst Zellkontakt
Wie 3D-Nanoelektroden beschaffen sein müssen, damit biologische Zellen optimal mit ihnen Verbindung aufnehmen können, das haben Jülicher Forscher untersucht. Als ideal erwies sich ein möglichst langer dünner Stiel mit einer breiten Kappe. Die Erkenntnisse sind etwa für die Entwicklung von Netzhaut-Implantaten und hochpräzisen Biosensoren interessant, mit denen sich Medikamente testen oder die Ursachen neurodegenerativer Erkrankungen erforschen lassen. Die Ergebnisse wurden in der Fachzeitschrift ACS Nano veröffentlicht.
Zellen besitzen die Fähigkeit, Fremdkörper zu umhüllen, um sie sich anschließend einzuverleiben. Der Prozess ermöglicht es der Zelle, Boten- und Nährstoffe aufzunehmen. Aber der Mechanismus ist auch ein Einfallstor für Viren und Bakterien. "Bei der Entwicklung von nanostrukturierten 3D-Oberflächen für bioelektronische Schnittstellen nutzen wir dieses Verhalten aus, um die Verbindung zwischen der Zellmembran und der Elektronik zu verbessern", erklärt Prof. Andreas Offenhäusser, Direktor des Jülicher Peter Grünberg Instituts, Bereich Bioelectronics (PGI-8 / ICS-8).
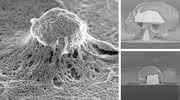
Die winzigen 3D-Nanoelektroden wirken auf biologische Zellen wie ein Köder, der schließlich von ihnen geschluckt wird. Doch auf welchen Köder, oder eher: auf welche Form, die Zellen am besten ansprechen, war bislang offen. Weltweit werden verschiedene Ansätze verfolgt. Einige beschränken sich auf Elektroden, die nur aus einem einfachen zylindrischen Stiel bestehen, andere sehen zusätzlich noch eine pilzähnliche Kappe am oberen Ende vor. Unter dem Fokussierten Ionenstrahl- und Rasterelektronenmikroskop konnten die Jülicher Biophysiker zeigen, dass die Wahl des Designs tatsächlich den Zellkontakt beeinflusst. Optimal ist ein möglichst langer dünner Stiel mit breiter Kappe, wie die Wissenschaftler mithilfe eines theoretischen Modells errechnet haben.
"Für eine Vielzahl von Anwendungen ist es wichtig, dass die Zelle sehr nah an der Elektrode anliegt. Schon der Abstand von einem zehntausendstel Millimeter reicht aus, und man kann nichts mehr messen", verdeutlicht Andreas Offenhäusser. Die Kopplung von lebendem Gewebe und anorganischer Halbleiterelektronik zu verbessern, ist eine der größten Herausforderungen bei der Entwicklung bioelektronischer Komponenten. Das Anwendungsspektrum reicht von Neuroprothesen, die eines Tages defekte Organe ersetzen könnten, bis hin zu hochpräzisen Sensorchips für In-Vitro-Experimente. Letztere ermöglichen es zunehmend, mithilfe einzelner Zellen, die sich auf dem Chip ansiedeln, preisgünstig, schnell und ethisch verträglich die Wirkung von Medikamenten zu überprüfen oder Prozesse zu untersuchen, die als Ursache für Hirnerkrankungen infrage kommen.
Originalpublikation:
Interfacing Electrogenic Cells with 3D Nanoelectrodes: Position, Shape, and Size Matter: Santoro F., Dasgupta S., Schnitker J., Auth T., Neumann E., Panaitov G., Gompper G., Offenhäusser A. ACS Nano, 2014 Jun 25 (published online ahead of print), DOI: 10.1021/nn500393p. Abstract: http://pubs.acs.org/doi/abs/10.1021/nn500393p
Ansprechpartner:
Prof. Dr. Andreas Offenhäusser
Peter Grünberg Institute / Institute of Complex Systems - Bioelectronics (PGI-8/ICS-8)
[email protected]