Signal zum Zelltod
Kristalle als Krankmacher
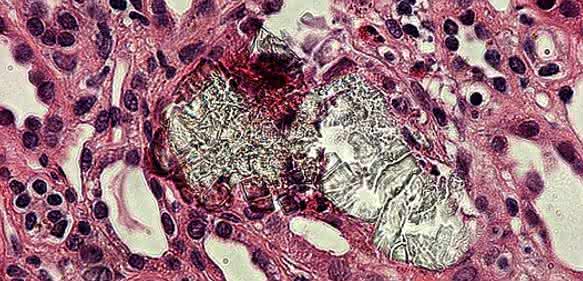
Bei Gicht, Atherosklerose und anderen Volkskrankheiten schädigen Kristalle Gewebe. Forscher um Hans-Joachim Anders zeigen nun, wie die Mikropartikel das Absterben von Zellen auslösen.
Bei verschiedenen weit verbreiteten Krankheiten sind Kristalle die Auslöser. Sie führen, wie etwa die Harnsäure-Kristalle bei Gicht, zu einer Abwehrreaktion des Immunsystems und lösen Entzündungen aus, zugleich verursachen sie das Absterben von Gewebezellen.
Ein Forscherteam um Prof. Hans-Joachim Anders von der Medizinischen Klinik und Poliklinik der LMU hat nun erstmals den Mechanismen dieses Kristall-vermittelten Zelltods identifiziert. Ihre Ergebnisse sind für viele Erkrankungen von Bedeutung, darunter neben Gicht auch Atherosklerose und manche Formen des akuten Nierenversagens. Sie sind aktuell in der Fachzeitschrift Nature Communications veröffentlicht.
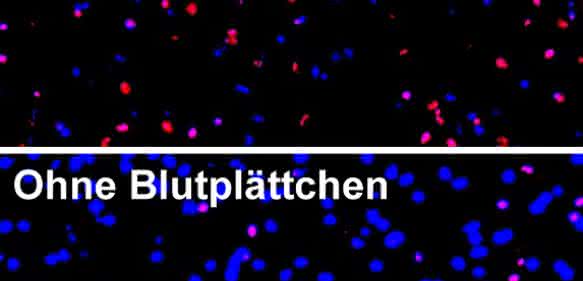
Kristalle schädigen das Gewebe und können zu einem Versagen betroffener Organe führen. Es wird vermutet, dass die von ihnen ausgelösten ganz verschiedenen Erkrankungen einen verbindenden Pathomechanismus haben. Bislang konzentrierte sich die Forschung vor allem darauf, wie Kristalle Entzündungen auslösen. Die Forscher um Hans-Joachim Anders konnten nun erstmals zeigen, dass die Kristalle bei Gewebezellen eine Form der regulierten Nekrose in Gang setzen. „Das galt bisher eher als passive Zellzerstörung. Es ist aber ein aktiv regulierter Mechanismus, der zum direkten Zelltod führt“, sagt Hans-Joachim Anders.
Neuer Ansatzpunkt für Medikamente
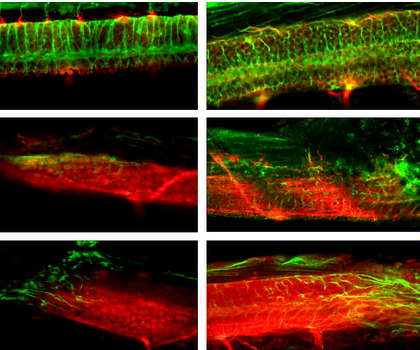
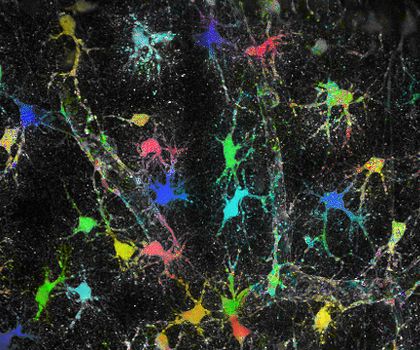
Die Forscher haben den molekularen Mechanismus unter anderem an Nieren- und Bindegewebszellen untersucht. Am Beispiel mehrerer Kristalle zeigen sie auf, dass die Mikropartikel den immer selben Signalweg aktivieren, der zum Zelltod führt. Ihre Daten weisen darauf hin, dass die Nekrose der Auslöser für das Entzündungsgeschehen ist.
Bislang wird auch bei der medizinischen Behandlung von Erkrankungen, die durch Kristalle ausgelöst werden, auf Entzündungshemmung gesetzt. Der von Hans-Joachim Anders und seinen Kollegen identifizierte Mechanismus bietet nun ein neues Ziel für die pharmakologische Forschung. „Der Signalweg könnte ein neuer Ansatzpunkt für Medikamente sein. Wird er unterbunden, würde das den durch Kristalle direkt ausgelösten Zelltod verhindern“, sagt Anders.
Der Studie zufolge müsste sich dadurch auch die Entwicklung einer chronischen Entzündung verhindern lassen. Ob sich daraus auch praktische Verbesserungen für die Behandlung von Patienten ergeben können, muss die weitere Forschung zeigen.
Publikation:
Cytotoxicity of crystals involves RIPK3-MLKL-mediated necroptosis: Mulay, S. R. et al. In: Nat. Commun. 7:10274, DOI: 10.1038/ncomms10274 (2016).
Ansprechpartner:
Prof. Dr. Hans-Joachim Anders
Medizinische Klinik IV
Klinikum der Universität München – Campus Innenstadt
Allgemeinmedizin und Nephrologie
E-Mail: [email protected]