Infektionsforschung
Bakterienkapsel im Reagenzglas nachgebaut
Manche Bakterien verfügen über eine Schutzhülle aus miteinander vernetzten Zuckermolekülen. Forscher haben diese Kapsel nun im Reagenzglas nachgebaut. Die Arbeit identifiziert auch mögliche Angriffspunkte für neue Medikamente.
Die Kapsel ist ein komplex aufgebautes Zucker-Polymer, in das sich manche Mikroorganismen hüllen können und die Bakterien sozusagen für das Immunsystem unsichtbar macht. Außerdem ist sie eine Barriere für Abwehrstoffe, etwa bestimmte Antibiotika. Könnte man die Bildung der Kapsel verhindern, würde das Krankheitserregern daher einen schweren Schlag versetzen. „Dennoch wissen wir noch erstaunlich wenig darüber, wie die Kapsel entsteht“, erklärt Prof. Dr. Tanja Schneider vom Institut für Pharmazeutische Mikrobiologie der Universität Bonn.
Die jetzt in der Zeitschrift „Nature Communications“ erschienene Studie ändert das ein Stück weit: Wissenschaftler der Universität Bonn und des Deutschen Zentrums für Infektionsforschung (DZIF) haben die Kapsel des weit verbreiteten Keims Staphylococcus aureus im Reagenzglas „nachgebaut“. Staphylokokken zählen zu den so genannten gram-positiven Bakterien. Diese zeichnen sich durch einen bestimmten Aufbau ihrer Zellwand aus. Außerdem verfügen sie über die Fähigkeit, eine Kapsel zu bilden.
Hülle nach dem „Zwiebel-Prinzip“
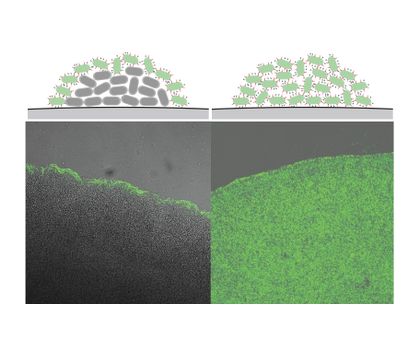
Staphylococcus ist – vereinfacht gesagt – von drei verschiedenen Hüllschichten umgeben. Die innerste davon ist die Membran, ein hauchdünnes fettähnliches Häutchen. An sie schließt sich eine Wand aus eng vernetzten Zucker-Peptid-Fasern an, dem so genannten Murein. Erst danach kommt, ganz außen aufgelagert, die Kapsel. Es war bereits bekannt, dass an ihrer Entstehung 16 verschiedene Enzyme beteiligt sind. Diese sind an und in der Membran befestigt und funktionieren nur in diesem Zustand – ein wesentlicher Grund, warum sie so schwer zu untersuchen sind. Dazu haben die Forscher die Kapsel-Enzyme isoliert, gereinigt und zusammen mit Membran-Bestandteilen in ein Reagenzglas gegeben. „Wir haben so die natürlichen Bedingungen nachgestellt“, erklärt Schneiders Mitarbeiter Dr. Marvin Rausch. „Auf diese Weise konnten wir die katalysierten Reaktionen analysieren, aber auch untersuchen, wie diese koordiniert werden.“
Dabei hat die Gruppe, zu der auch Forscher aus England und den USA zählten, einige unerwartete Entdeckungen gemacht. So ist die Kapsel-Synthese auf eine Art Lieferservice angewiesen. Dieser bringt Ausgangsstoffe zu den entsprechenden Enzymen. Interessanterweise wird dieser Bringdienst aber auch noch für einen anderen Zweck genutzt: als "Zulieferer" für die Mureinwand-Synthese. „Diese Wand ist für die meisten Bakterien lebenswichtig“, betont Schneider. „In Staphylococcus aureus darf die Kapsel daher erst synthetisiert werden, wenn die Wand fertig ist.“
Ein Enzym namens PknB sorgt dafür, dass diese Abfolge eingehalten wird. Solange der "Lieferservice" noch Murein-Bestandteile transportiert, sorgt PknB dafür, dass die Kapsel-Synthese abgeschaltet bleibt. Danach aber switcht das Bakterium radikal um: Sobald die Herstellung der Kapsel beginnt, springt ein anderes Enzym namens CapA an. Dieser Katalysator wird durch Kapsel-Zwischenprodukte zusätzlich aktiviert. Dadurch kommt eine positive Feedback-Schleife in Gang, die CapA gewissermaßen zu Höchstleistungen anspornt.
Suche nach Wirkstoffen
Sowohl CapA als auch PknB übernehmen wichtige Funktionen bei der Kapsel-Synthese. Sie eignen sich daher womöglich als Ziel für neue Medikamente. „Außerdem haben wir ein Molekül identifizieren können, das die Kapsel an der Murein-Wand verankert“, sagt Schneider. „Möglicherweise eröffnet sich dadurch eine weitere therapeutische Option.“
In einem nächsten Schritt wollen die Wissenschaftler in riesigen Substanz-Bibliotheken nach Wirkstoffen suchen, die sich gegen die gefundenen Strukturen richten. Bis daraus neue Medikamente entstehen, werden aber wohl selbst im Idealfall noch viele Jahre vergehen. „Dennoch ist diese Arbeit ausgesprochen wichtig“, erklärt Schneider. „Zwar ist es durch verschiedene Maßnahmen gelungen, Infektionen durch Staphylokokken etwas besser in den Griff zu bekommen. Die Erfahrung lehrt aber, dass wir uns darauf nicht ausruhen dürfen: Irgendwann entstehen neue Resistenzen, und dann sollten wir vorbereitet sein.“
Publikation:
Marvin Rausch, Julia Deisinger, Hannah Ulm, Anna Müller, Wenjin Li, Patrick Hardt, Xiaogang Wang, Xue Li, Marc Sylvester, Marianne Engeser, Waldemar Vollmer, Christa E. Müller, Hans Georg Sahl, Jean Claire Lee & Tanja Schneider: Coordination of capsule assembly and cell wall biosynthesis in Staphylococcus aureus; Nature Communications; https://doi.org/10.1038/s41467-019-09356-x
Quelle: Universität Bonn