Arteriosklerose, Krebs, Adipositas
Neuer genetischer Faktor bei defekten Makrophagen entdeckt
Wissenschaftler der Universitätsmedizin Leipzig ordnen einen neuen genetischen Faktor funktionell veränderten Makrophagen zu. Ihre Studie liefert Hinweise auf die Entstehung von Adipositas und Herz-Kreislauf-Erkrankungen.
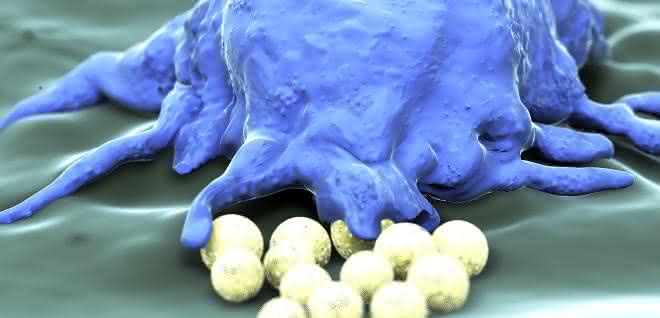
Sie überleben nur 30 bis 90 Tage im menschlichen Organismus und erledigen in dieser kurzen Zeit lebenswichtige Aufgaben: Makrophagen, große bewegliche Zellen, sind Bestandteil der Immunantwort des Körpers. Sie entwickeln sich aus Monozyten im Knochenmark und zirkulieren im Blutkreislauf. Wenn Krankheitserreger wie Bakterien oder Viren in den Körper gelangen, werden sie von Makrophagen erkannt und zerstört. Zudem bauen sie Tumorzellen ab und fördern die Wundheilung. Diese Aufgaben erledigen Makrophagen jedoch nicht mehr richtig, wenn ein bestimmtes Gen nicht exprimiert, also abgelesen und in ein Protein übersetzt wird.
Makrophagen in der Petrischale untersucht
Dieses Gen, das TRIB1-Gen, haben die Wissenschaftler in ihrer Studie gezielt ausgeschaltet und das Verhalten der Makrophagen beobachtet. Dazu wurden die Makrophagen aus Stammzellen des Knochenmarks gewonnen und in der Petrischale, also in vitro, untersucht. "Wir haben uns die Funktionsweise der Zellen angeschaut in denen das Gen aktiv war und mit Zellen verglichen, die kein funktionsfähiges TRIB1-Gen aufwiesen", sagt Erstautorin Lilli Arndt, die die Untersuchung im Rahmen ihrer Doktorarbeit an der Universität Leipzig durchführte und dazu am Institut für Laboratoriumsmedizin, Klinische Chemie und Molekulare Diagnostik (ILM) des Universitätsklinikums Leipzig forscht. "Die Ergebnisse zeigen, dass die Funktion der Makrophagen beeinträchtigt ist, wenn das Gen bei einer Aktivierung der Makrophagen nicht exprimiert werden kann."
Weniger mobil, mehr Appetit
Zum einen waren die Makrophagen ohne TRIB1-Gen weniger mobil. Normalerweise bewegen sich die Zellen aktiv fort, wenn sie stimuliert werden. In der Untersuchung waren die Makrophagen jedoch weniger bewegungsfreudig, was auf eine Dysfunktion schließen lässt. Zum anderen nahmen die Fresszellen ohne das TRIB1-Gen vermehrt cholesterinhaltige Partikel (Lipoproteine) aus ihrer Umgebung auf. "TRIB1 wurde bereits als Kandidatengen der Arteriosklerose identifiziert. Unsere Befunde zu TRIB1 im Makrophagen liefern Hinweise auf eine mögliche Funktion bei der Entstehung der Arteriosklerose. Hier wird überschüssiges Cholesterin in der Arterienwand von Makrophagen aufgenommen, was zur Bildung von Schaumzellen und einer Verengung der Gefäßwand führt", erklärt Prof. Dr. Ralph Burkhardt vom ILM, der die Studie betreute.
Zellen können sich nicht mehr vollständig differenzieren
Makrophagen können in zwei Erscheinungsformen auftreten: entweder entzündungsfördernd, also pro-inflammatorisch, oder entzündungshemmend, auch anti-inflammatorisch genannt. Während entzündungsfördernde Fresszellen nach Eindringen eines Erregers weitere Immunzellen zum Infektionsort anlocken und für eine stärkere Durchblutung des betroffenen Gewebes sorgen, sind entzündungshemmende Makrophagen nach der Bekämpfung des Krankheitserregers dafür zuständig, dass die Entzündung wieder abklingt und sich die aktivierten Zellen abschalten. Die Leipziger Forscher konnten in ihrer Untersuchung nun zeigen, dass die Zellen ohne Expression des TRIB1-Gens eine der beiden Erscheinungsformen nicht mehr in Gänze annehmen konnten. "Die Makrophagen produzieren dann weniger Stoffe, die die Krankheitserreger abtöten, wie beispielsweise Stickstoffmonoxid. Damit sind sie wahrscheinlich vermindert fähig, eine adäquate Immunreaktion auszulösen", so Arndt.
Wichtige Erkenntnisse für Adipositas- und Arteriosklerose-Forschung
Die Ergebnisse aus der Grundlagenforschung können praktische Relevanz vor allem für Herz-Kreislauf-Erkrankungen wie Arteriosklerose, aber auch für Adipositas haben. Denn auch im Fettgewebe spielen Makrophagen eine wichtige Rolle. Sie vernichten abgestorbene Zellen und produzieren bestimmte Stoffe, die direkt auf das Fettgewebe wirken. Untersuchungen konnten bislang zeigen, dass bei adipösen Menschen eher entzündungsfördernde Makrophagen im Fettgewebe zu finden sind, bei normalgewichtigen Menschen eher entzündungshemmende. Weitere Studien können nun herausstellen, welchen Effekt das TRIB1-Gen auf das Fettgewebe bei Adipositas hat. Auch in Bezug auf die Arteriosklerose analysieren die Leipziger Forscher in weiteren Studien, wie die Veränderung des TRIB1-Gens die Krankheitsentstehung beeinflussen kann.
Unterstützt wurde die Untersuchung in Zusammenarbeit mit dem Institut für Anatomie der Universität Leipzig vom DFG-Sonderforschungsbereich "Mechanismen der Adipositas" und von der Stiftung für Pathobiochemie und Molekulare Diagnostik der Deutschen Geselleschaft für Laboratoriumsmedizin.
Originalveröffentlichung in "Journal of Biological Chemistry":
"Tribbles homolog 1 deficiency modulates function and
polarization of murine bone marrow-derived macrophages", DOI 10.1074/jbc.RA117.000703.
Weitere Informationen:
Prof. Dr. Ralph Burkhardt
Medizinische Fakultät
Institut für Laboratoriumsmedizin, Klinische Chemie und Molekulare Diagnostik
Telefon: +49 341 97-22471
E-Mail: [email protected]