Untersuchungen an einem Chlorophyllprotein
Wie Pflanzen Chlorophyll binden
Forscher haben untersucht, wodurch sich bei dem wasserlöslichen Chlorophyllprotein die Präferenz für eine der beiden Chlorophyll-Varianten, also die Bindungsselektivität ändert.
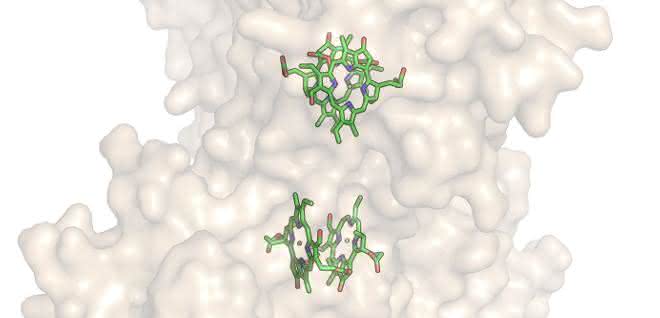
Es gibt zwei Varianten des grünen Pflanzenfarbstoffs: Chlorophyll a und Chlorophyll b, die strukturell einander sehr ähnlich sind, aber unterschiedliche Farben aufweisen - blaugrün beziehungsweise gelbgrün. Beide Farbstoffe haben in der Photosynthese verschiedene Aufgaben; daher werden sie sehr selektiv von den Photosynthese-Proteinen der Pflanzen gebunden. Wie jedoch diese Pflanzenproteine die beiden Chlorophylle mit ihren kleinen Strukturunterschieden erkennen und selektiv binden können, das war bisher weitgehend unklar.
Forscherinnen und Forscher der Johannes Gutenberg-Universität Mainz (JGU) sind zusammen mit zwei japanischen Kollegen der Lösung dieses Rätsels ein Stück näher gekommen. Das Team um Prof. Dr. Harald Paulsen vom Fachbereich Biologie verwendete das sogenannte Wasserlösliche Chlorophyllprotein aus Blumenkohl und aus Virginischer Kresse als Modellprotein. Dieses Protein besitzt nur eine einzige Chlorophyll-Bindestelle pro Proteinmolekül und kann beide Varianten des Farbstoffs binden. Durch Variation der Aminosäuren in der Chlorophyll-Bindestelle änderte sich die Präferenz des Proteins für eine der beiden Farbstoff-Varianten. Im Extremfall machte der Austausch einer einzigen Aminosäure aus einem Chlorophyll-b- ein Chlorophyll-a-bindendes Protein; dabei änderten sich die relativen Bindestärken 40-fach. „Das erklärt noch nicht alles zur Spezifität für Chlorophyll a oder Chlorophyll b im Photosynthese-Apparat“, so Paulsen. „Aber unsere Ergebnisse liefern wertvolle Hypothesen, die sich jetzt an Photosynthese-Proteinen testen lassen. Auf längere Sicht können diese Ergebnisse dazu beitragen, die Lichtsammlung in der Solartechnik zu verbessern.“
Einer der Erstautoren der Veröffentlichung in „Nature Plants“ ist Dr. Alessandro Agostini; er erhielt seinen Doktortitel für eine Arbeit zum Wasserlöslichen Chlorophyllprotein gleichzeitig von der JGU (Arbeitsgruppe Paulsen) und der Universität Padua in Italien (Gruppe von Prof. Dr. Donatella Carbonera). „Dies ist ein schönes Beispiel für eine erfolgreiche internationale Zusammenarbeit“, stellt Paulsen fest, „nicht nur im Sinne der Forschung, sondern auch bei der Begleitung eines Promotionsstudiums.“ Die Arbeit wurde von der Deutschen Forschungsgemeinschaft gefördert.
Publikation:
Daniel M. Palm et al.: Chlorophyll a/b binding-specificity in Water-Soluble Chlorophyll Protein; Nature Plants, 8. Oktober 2018. DOI: 10.1038/s41477-018-0273-z; www.nature.com/articles/s41477-018-0273-z