Überkritische Flüssigkeitschromatographie
Chirale Trennung von Pestiziden durch SFC-CD-MS-Systeme
Zur überkritischen Flüssigkeitschromatographie (SFC) wird als Hauptbestandteil der mobilen Phase ein überkritisches Fluid (am häufigsten CO2) benötigt. Durch die inhärenten Eigenschaften wie niedrige Viskosität und hohe Diffusionsfähigkeit des überkritischen CO2 kann die SFC schneller und effizienter sein als die herkömmliche HPLC. SFC kann schnellere Durchflussraten mit kürzeren Analysezeiten erzielen, ohne die Notwendigkeit, mit sehr hohen Drücken, wie bei UHPLC, zu arbeiten.
Die Komponenten in einem SFC-System sind die gleichen wie in einem HPLC-System plus eine Hochdruck-Durchflusszelle für den Detektor und einem Gegendruckregler (BPR – Back Pressure Regulator). Der BPR sichert einen kontrollierten Druck auf dem Säulenausgang. So können die überkritischen Bedingungen genau aufrechterhalten werden, wodurch der BPR zu einem wesentlichen Bestandteil des Systems wird.
Etwa 30 % der derzeit weltweit verwendeten Pestizide sind chirale Isomere mit einem oder mehreren chiralen Zentren [1]. Es ist bekannt, dass die biologischen Aktivitäten, die unerwünschte toxische Wirkung auf nicht anvisierte Organismen, die Stoffwechselrate sowie der biologische Abbau in der Umwelt bei den Enantiomeren von chiralen Pestiziden unterschiedlich sein können. Obwohl die Verwendung der effektiveren und sichereren Enantiomere wünschenswert wäre, werden die meisten chiralen Pestizide – wegen des komplizierten Verfahrens und der hohen Kosten der Herstellung des puren Enantiomers – als Racemate vermarktet und verwendet.
Generell ist die chirale Trennung durch HPLC, GC und SFC eine der wichtigsten analytischen Methoden bei der Syntheseentwicklung von einzelnen Enantiomeren [2]. Obwohl die HPLC aufgrund ihrer einfachen Handhabung immer noch die chromatographische chirale Analyse dominiert, hat die SFC Vorteile, wie kürzere Analysezeiten und signifikante Reduzierung sowohl des Lösungsmittelverbrauchs als auch der Kosten.
In dieser Studie wurde eine chirale Trennmethode für Pestizide unter Verwendung von SFC mit Zirkulardichroismusdetektor (CD) und Massenspektrometer (MS) entwickelt. Der CD-Detektor liefert gleichzeitig Zirkulardichroismus- und UV-Absorptionssignale und ermöglicht die selektive Identifizierung der CD-Polarität jedes Enantiomers. MS-Spektren werden verwendet, um zwischen chiralen Isomergruppen mit dem gleichen m/z-Wert von anderen Komponenten einschließlich Verunreinigungen zu unterscheiden. Der hochempfindliche Nachweis mit UV, CD und MS kann bei der Analyse der chiralen Trennungen in der Entwicklung der Synthese eines reinen Pestizid-Enantiomers zum Einsatz kommen.
Experiment
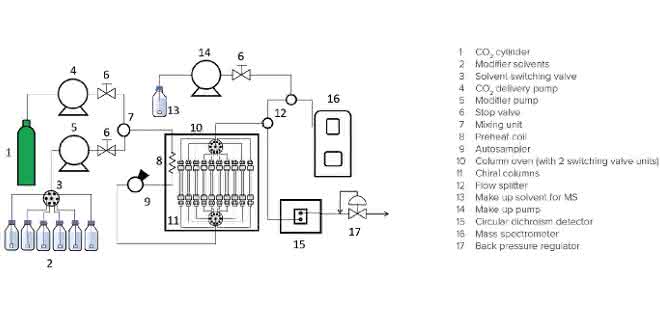
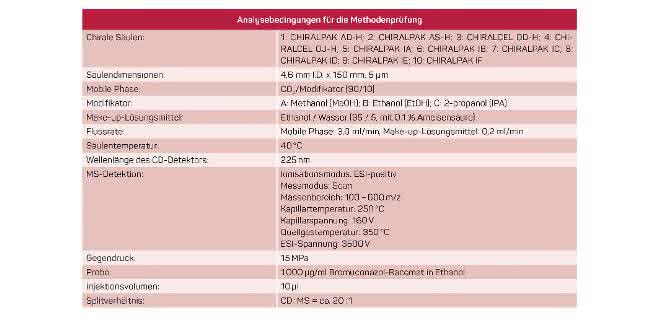
Im Folgenden wird die Anwendung der SFC an Bromuconazol, eine Art Triazol-Fungizid [2], beschrieben. In dem Experiment wurde das “JASCO SFC-CD-MS”-System (Bild 1) verwendet. Mit Hilfe eines Splitters mit einem PEEK-beschichteten Kapillarröhrchen wird der Fluss von der chiralen Säule kommend in zwei Kanäle aufgeteilt, jeweils einer zu den CD- und MS-Detektoren. Der CD-Detektor liefert gleichzeitig die CD- und UV-Signale. Dieses System ermöglicht die automatisierte Durchführung einer Methodenprüfung („Method Scouting”) von Säulen und mobilen Phasen.
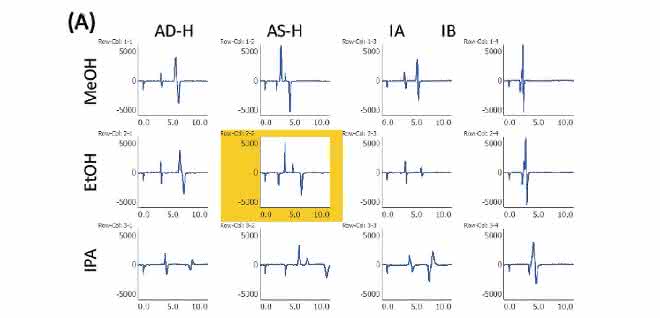
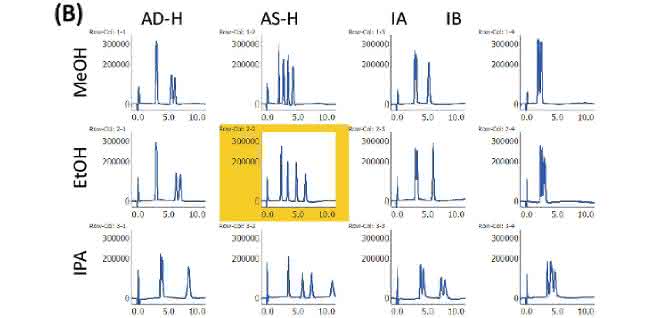
Racemisches Bromuconazol mit zwei chiralen Zentren kann unter Verwendung einer chiralen Säule in vier Isomerenpeaks getrennt werden. Bild 2 zeigt die ausgewählten Ergebnisse der Methoden-Prüfung für mobile Phasen und Säulen. Die beste Trennung wurde unter Verwendung von Ethanol und der Säule „CHIRALPAK AS-H“ (im Bild gelb hervorgehoben) beobachtet. In den folgenden Experimenten wurde diese Säule/Eluent-Kombination verwendet.
Untersuchung mit CD-Detektor und MS
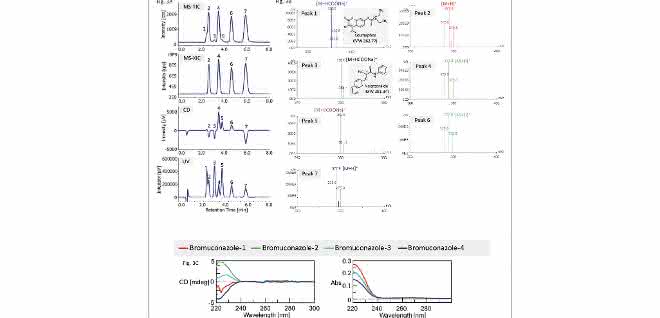
Bild 3 zeigt die Ergebnisse zu den Untersuchungen eines Bromuconazol-Standards, der mit zwei zusätzlichen Pestiziden (Coumaphos und Naproanilid) versetzt ist, die durch CD-Detektor und Massenspektrometer als Verunreinigungen nachgewiesen wurden. Bild 3A zeigt das Gesamtionenchromatogramm (TIC) von 100 bis 600 m/z, das extrahierte Ionenchromatogramm (XIC) von m/z 378,0 sowie CD- und UV-Chromatogramme. Bild 3B zeigt die MS-Spektren jedes in Bild 3A beschriebenen Peaks. Wie in dieser Abbildung gezeigt, können die Bromuconazol-Isomere und andere Verunreinigungen klar unterschieden werden. Bromuconazol-Isomere (Peaks 2, 4, 6 und 7) weisen Ähnlichkeiten in ihren Spektren auf, und ein protoniertes Molekülion ([M + H]+) wurde bei m/z 377,8 als Basenpeak im Massenspektrum jedes Isomerpeaks beobachtet. Natriumformiat-Adduktionen ([M + HCOONa]+) von Coumaphos und Naproanilid werden auch bei m/z 430,9 (Peak 1) und m/z 360,0 (Peaks 3 und 5) beobachtet. Bild 3C zeigt die mit angehaltenem Fluss aufgenommenen CD- und UV-Spektren der Peaks von Bromuconazol-Standard. Bei den Spektralmessungen wird ein 6-Wege-Umschaltventil mit zwei Positionen verwendet, um den Durchfluss umzuleiten und jeden Peak in der Durchflusszelle für eine statische Spektrumaufnahme zu „parken“. Die Spektren von Bromuconazol-1, 2, 3 und 4 entsprechen den Peaks 2, 4, 6 und 7 in der Abb. 3A. Gemäß den CD-Informationen aus den Bildern 3A und 3C werden die Peaks 2 und 6 der Bromuconazol-Isomere aufgrund ihrer CD-Polarität und ihres Wellenlängenmaximums als Enantiomerenpaar beurteilt. Auch die Peaks 4 und 7 müssten demnach ein Enantiomerenpaar sein.
Zusammenfassung
Die beschriebene chirale Trennmethode durch SFC mit CD-Detektoren und Massenspektrometer kann für Pestizide eingesetzt werden: Gesamt- ionenchromatogramme TIC, CD- und UV-Detektion machen die Identifizierung chiraler Isomere und anderer Verunreinigungen mittels chiraler Trennung möglich.
Literaturhinweise/Quellen:
[1] B. S. Sekhon, J. Pestic. Sci, 2009, 34 (1), 1-12.
[2] V. Pérez-Fernández, M. Á. Garciá, M. L. Marina, J. Chromatogr. A, 2011, 1218, 6561-6582.
[3] Satoe Iijima et al.: High Sensitive and Comprehensive Detection for Chiral Separation of Pesticide using SFC-CD-MS; Poster für SFC Asia 2017
JASCO Deutschland GmbH
Kontakt: Thomas Machate
[email protected]
www.jasco.de