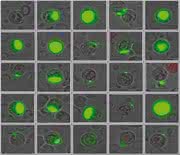
Tumorstammzellen
Die gefährlichsten Zellen eines Tumors diagnostisch nutzen
Ihre Existenz galt lange Zeit als umstritten. Sie verfügen über typische Stammzelleigenschaften, können sich in verschiedene Gewebe ausdifferenzieren und sich selbst erneuern. Sie sind in der Lage, Tochterzellen zu generieren, die selbst Stammzelleigenschaften besitzen und sogar über ein größeres Differenzierungspotenzial verfügen können als sie selbst. Die Rede ist von den Tumorstammzellen.
Sie sind diejenigen Zellen eines Tumors, die für den permanenten Nachschub an Tumorzellen sorgen und den Tumor somit am Leben erhalten. Sie können ihn sogar verlassen, um sich über die Blutbahn im gesamten Körper des Patienten zu verbreiten und sich unter Umständen in fremdem Gewebe anzusiedeln und hier Metastasen zu bilden.
Erst jüngst gelang es niederländischen Forschern unter Leitung von Hans Clevers von der Universität Utrecht nachzuweisen, dass Krebsstammzellen bereits in Darmpolypen - einer Vorstufe für Darmkrebs - aktiv sind und dass diese Zellen das Wachstum von Darmpolypen fördern. Die Praxis nähert sich damit zunehmend der Theorie, die im Hinblick auf die Tumorstammzellen bereits eine lange Historie vorweisen kann.
Ihren Ursprung nahm sie 1997. Die kanadischen Wissenschaftler Dominique Bonnet und John Dick hatten in ihrer Publikation "Human acute myeloid leukemia is organized as a hierarchy that originates from a primitive hematopoietic cell" die wachstumsbefähigten und aggressiven Zellen erstmals in den Fokus gerückt. Sie hatten die Tumorstammzellen - neben der Entstehung von Tumoren - auch für die Resistenz maligner Tumore gegen bestimmte Therapien sowie für die häufigen Rezidive bei Krebserkrankungen verantwortlich gemacht. Ein Verdacht, der sich nach jahrelanger Forschung inzwischen bestätigt hat. Der Einfluss der Tumorstammzellen auf die Entwicklung von Tumoren und ihre Bedeutung für die Ausgestaltung von Therapien ist heute Gegenstand verschiedenster Studien und von besonderer klinischer Relevanz.
Tumorstammzellen sind die gefährlichsten Zellen in einem Tumor. Sie haben nicht nur maßgeblichen Einfluss auf die Aggressivität eines Tumors. Sie weisen darüber hinaus eine beeindruckende Resistenz gegen viele Krebstherapien auf. Diese Widerstandsfähigkeit ist auf verschiedenste Verteidigungstechniken zurückzuführen, die die Zellen - abhängig vom jeweiligen Tumortyp - entwickeln. Einige der Stammzellen verfügen beispielsweise über spezielle Moleküle auf ihrer Oberfläche, die im Rahmen von Chemotherapien eingesetzte Gifte aus dem Zellinneren heraus befördern können. Andere weisen Stoffe auf, die chemotherapeutisch bedingte Schäden an ihrem Erbgut reparieren. Und wiederum andere Krebsstammzellen verbarrikadieren sich in einem Schutzraum im Körper. Sie stellen sich schlafend und lassen die meisten Chemotherapien ins Leere laufen. Letztere entfalten häufig nur auf sich schnell teilende Zellen die erhoffte Wirkung.
Etwa ein zweistelliger Prozentsatz der Tumorstammzellen verbleibt daher nach Austherapierung im Körper eines Patienten. Dabei scheint der Prozentsatz mit der Tumorentwicklung zu korrelieren. Während in Studien kleine, noch gut differenzierte Tumore nur wenige der Zellen mit Stammzelleigenschaften aufwiesen, bestehen therapieresistente Metastasen häufig fast ausschließlich aus den wachstumsbefähigten Tumorstammzellen. Im Zusammenspiel mit den ohnehin im Blutkreislauf zirkulierenden Tumorzellen, die ebenfalls ein metastaseninduzierendes Potenzial aufweisen können, sind die Stammzellen augenscheinlich in der Lage, nach scheinbar erfolgreicher Therapie zu Rückfällen sowie zur Bildung von Metastasen führen.
Es ist somit vielversprechend, die Tumorstammzellen mit entsprechend empfindlichen Diagnostik-Verfahren aufzuspüren, um sie im Rahmen einer Therapie gezielt vernichten zu können. Krebsstammzellen können inzwischen bei zahlreichen soliden Tumoren nachgewiesen - etwa bei Darm-, Brust- und Prostatakarzinomen - und mittels ihrer Zelloberflächenrezeptoren charakterisiert werden. Ein entsprechendes Verfahren, mit dem dieser Nachweis anhand des Blutbildes gelingt, ist das maintrac-Verfahren, das bereits bei der Detektion, Quantifizierung und Charakterisierung von zirkulierenden, epithelialen Tumorzellen (CETCs) weltweit etabliert ist.
Dabei werden die tumorverdächtigen Zellen zunächst durch Zugabe fluoreszierender, antihumaner epithelialer Antikörper markiert, die an das auf mehr als 95 % der Tumorzellen vorhandene Epitheliale Cytoadhäsions-Molekül (EpCAM) andocken. Anschließend werden sie auf einem Trägermaterial anhand der Laser-Scanning-Cytometrie oder mit Bildanalyse automatisiert erfasst. Die Identifizierung der Zellen, die über Stammzelleigenschaften verfügen, erfolgt über eine Kultivierung der gesamten Zellen einer Blutprobe für bis zu 21 Tage in einem Medium, das das Wachstum epithelialer Zellen begünstigt. Dadurch vermehren sich die Zellen, die zu klonalem Wachstum befähigt sind, und bilden kugelige Zellaggregate (Tumorsphären). Diese Sphären weisen die typischen Biomarker von Stammzellen auf, wie geringe Expression von CD24, hohe Expression von CD44 und ALDH1. Aber auch nanogenetische Analysen anhand einzelner Tumorzellen können zur Identifizierung der Stammzellen herangezogen werden.
Um schließlich nachhaltige Heilungserfolge zu erzielen, muss die angewandte Krebstherapie in jedem Fall die Stammzellpopulation eines Tumors wirksam bekämpfen. Allerdings scheinen die Stammzellen wie die Tumore selbst äußerst heterogen zu sein. Vergleichende Expressionsanalysen deuten auf unterschiedliche Subgruppen hin, die wahrscheinlich von verschiedenen Krebsstammzellen erzeugt werden. Eine weitere molekulare Charakterisierung der identifizierten Tumorstammzellen ist demnach notwendig. Mit dem maintrac-Verfahren lassen sich so beispielsweise wichtige Erkenntnisse über deren Oberflächenbeschaffenheit - insbesondere bestimmten Rezeptoren - gewinnen, die für die Ausgestaltung der Therapie relevant sind.
Mit maintrac wird anhand der dem Patienten entnommenen Blutproben die tumorstammzellsuppressive Wirkung verschiedener Medikamente in-vitro untersucht. Durch entsprechende Chemosensivitätstests werden dabei die Substanzen ermittelt, die in der Lage sind, die Tumorstammzellen abzutöten. Um die Chemosensitivität der in der Probe vorhandenen Tumorstammzellen festzustellen, wird durch Zugabe der für eine Therapie in Frage kommenden Medikamente analysiert, wie viele der Zellen prozentual absterben. Diese systematische Suche unter den Wirkstoffen, die gezielt die Stammzellen unter den Tumorzellen angreifen, ist ein eleganter Weg, der zu einer gezielteren Therapie gerade bei einer der aggressiven Stammzell-Subgruppen führen und denjenigen Patienten mit einer besseren Prognose eine belastende Chemotherapie ersparen kann.
Fazit
Gerade weil viele der Standard-Chemotherapien gegen Tumorstammzellen wirkungslos sind, ist es entscheidend, den diagnostischen Nutzen der gefährlichsten Zellen eines Tumors zu erschließen. Die Nachweis- und Charakterisierungsmöglichkeiten, die maintrac auch bei den Tumorstammzellen bietet, ermöglicht dies. Behandelnde Ärzte sind somit noch besser in der Lage, Krebstherapien entlang den individuellen Anforderungen des Patienten und seinen spezifischen Tumorstammzellen zu entwickeln und damit noch wirksamere Behandlungsformen zu schaffen. Im Ergebnis stehen weitere Verbesserungen der Heilungschancen der betroffenen Patienten sowie eine deutliche Minimierung der von den Tumorstammzellen ausgehenden Rückfallrisiken.
Dr. med. Ulrich Pachmann
Kurpromenade 2, 95448 Bayreuth,
Tel. +49(0)921/850200,
[email protected]