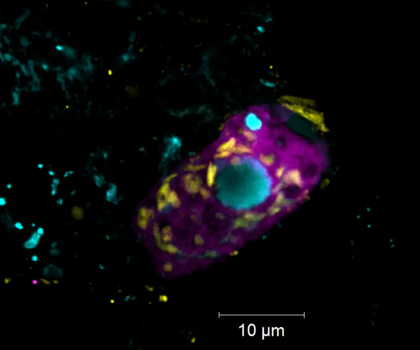
Die Effekte bakterieller Eiskeime
Bakterien fördern die Bildung von Eiskristallen
Der Gefrierpunkt von Wasser ist alles andere als eine eindeutige Sache. Kleine Tröpfchen aus reinstem Wasser etwa erstarren erst bei -37 °C zu Eis. Damit sich knapp unter 0 °C bereits Eiskristalle bilden, sind Kristallisationskeime wie etwa Bakterien nötig, die auf ihrer Oberfläche eisbildende Proteine aufweisen.
Den molekularen Mechanismus, über den die Proteine Wassermoleküle erstarren lassen, haben nun Forscher der Max-Planck-Institute für Chemie und für Polymerforschung aufgeklärt. Demnach erzeugen die Proteine geordnete Strukturen im Wasser und leiten Wärme ab. Die Erkenntnisse helfen nicht nur, die Bedingungen besser zu verstehen, unter denen Frostschäden an Pflanzen entstehen. Da die Bakterien auch in der Atmosphäre vorkommen, wo sie ebenfalls die Bildung von Eiskristallen fördern, spielen sie auch eine Rolle bei der Entstehung von Wolken und Niederschlag – einem großen Unsicherheitsfaktor in Wetter- und Klimavorhersagen.
Bei 0 °C gefriert ein Wassertropfen nie. Bei der Temperatur, die landläufig als Gefrierpunkt bekannt ist, bildet Wasser nur Eis, wenn es mit größeren Oberflächen Kontakt hat, in denen sich viele und große eisbildende Stellen befinden – etwa in einem Gefäß oder einem See. In Wassertropfen fördern Bakterien gezielt die Eisbildung, und zwar durch bestimmte Proteinmoleküle an ihrer Oberfläche, was bereits seit längerem bekannt ist. Weitgehend unverstanden waren bisher jedoch die molekularen Mechanismen, die dazu führen.
Max-Planck-Forscher haben nun aufgedeckt, was genau an der Bakterienoberfläche zwischen den Wasser- und den Proteinmolekülen geschieht. Ein Team um Tobias Weidner, Leiter einer Forschungsgruppe am Max-Planck-Institut für Polymerforschung, und Janine Fröhlich-Nowoisky, die eine Arbeitsgruppe am Max-Planck-Institut für Chemie leitet, zeigen, auf welche Weise eisaktive Bakterien – so der Fachbegriff – den Ordnungszustand und die Dynamik von Wassermolekülen beeinflussen.
Wie die Mainzer Forscher gemeinsam mit amerikanischen Kollegen in der neuesten Ausgabe des Wissenschaftsmagazins „Science Advances“ berichten, erzeugt die Wechselwirkung mit bestimmten Aminosäuresequenzen der Proteinmoleküle im Wasser Bereiche mit erhöhter Ordnung und stärkeren Wasserstoffbrückenbindungen. Zudem nehmen die Proteine Wärmeenergie aus dem Wasser auf und leiten sie weiter in das Bakterium. Dadurch können sich die Wassermoleküle schneller zu einem Eiskristall zusammen lagern.
Eisaktive Bakterien sind für Wissenschaftler aus mehrfacher Sicht von großem Interesse. Zum einen können sie Frostschäden an der Oberfläche von Pflanzen verursachen. Zum anderen können die Bakterien vom Wind in die Luft getragen werden. Dort wirken sie nicht nur als Kristallisations-, sondern auch als Kondensationskeime, so dass sie die Bildung von Schnee und Regen auslösen und so den Wasserkreislauf beeinflussen können.
Die Verbreitung von eisaktiven Bakterien und anderen Bioaerosolpartikeln in der Atmosphäre und ihr Einfluss auf die Bildung von Wolken und Niederschlag ist ein besonders vieldiskutiertes Thema in der aktuellen Klima- und Erdsystemforschung. Erkenntnisse, worauf die eisbildende Wirkung der Bakterien beruht, könnten helfen, ihre Rolle im Klimasystem besser zu verstehen.
Um zu verstehen, wie die Eiskristallbildung durch bakterielle Proteine angeregt wird, konzentrierten sich die Mainzer Forscher auf das eisaktive Bakterium Pseudomonas syringae. Dieses Bakterium löst schon bei -2 °C die Eisbildung in Wassertropfen aus. Zum Vergleich: Enthalten Wassertropfen nur Mineralstaub oder Ruß als Kondensationskeime für die Eiskristallbildung, setzt der Gefrierprozess erst ab Temperaturen von etwa -15 °C ein. In abgetöteter Form wird Pseudomonas syringae deshalb bereits als „Snomax“ kommerziell zur Produktion von Kunstschnee eingesetzt.
Für ihre Untersuchungen setzten die Wissenschaftler die sogenannte Summenfrequenzspektroskopie ein. Diese ermöglicht es, mittels Laserstrahlen gezielt die Wassermoleküle an der Bakterien- beziehungsweise Proteinober-fläche zu untersuchen.
Dank der neuen Ergebnisse scheint es nun möglich, die Eisbildungsmechanismen der Bakterien zu imitieren und im Labor künstlich nachzubauen und so für eine Reihe weiterer Anwendungen nutzbar zu machen. „In Zukunft wäre es nun denkbar, künstliche, nanostrukturierte Oberflächen und Partikel herzustellen, mit deren Hilfe die Bildung von Eis gezielt beeinflusst und kontrolliert werden könnte“, sagt Tobias Weidner.
Angespornt durch die positiven ersten Ergebnisse werden die beiden Max-Planck-Forschergruppen ihre Zusammenarbeit ausweiten. „Wir planen, zum einen die bakteriellen Eisproteine isoliert zu untersuchen. Derzeit finden die Untersuchungen noch an ganzen Bakterienzellen und Zellfragmenten statt. Zum anderen möchten wir die Analysen auf pilzliche Eiskeime erweitern“, erklärt Janine Fröhlich-Nowoisky, deren Arbeitsgruppe auf die Charakterisierung biologischer Eiskeime spezialisiert ist und über eine umfassende Kultursammlung, nicht nur von eisaktiven Bakterien, sondern auch von eisaktiven Pilzen, verfügt.
Originalpublikation:
„Ice-nucleating bacteria control the order and dynamics of interfacial water”: Ravindra Pandey, Kota Usui, Ruth A. Livingstone, Sean A. Fischer, Jim Pfaendtner, Ellen H. G. Backus, Yuki Nagata, Janine Fröhlich-Nowoisky, Lars Schmüser, Sergio Mauri, Jan F. Scheel, Daniel A. Knopf, Ulrich Pöschl, Mischa Bonn, Tobias Weidner. Science Advances, DOI: 10.1126/sciadv.1501630.
Kontakt:
Dr. Tobias Weidner
Max-Planck-Institut für Polymerforschung
E-Mail: [email protected]
Dr. Janine Fröhlich-Nowoisky
Max-Planck-Institut für Chemie
E-Mail: [email protected]